Agua hiperionizada : filtración, compatibilidad de los medios filtrantes y explicaciones fisicoquímicas detalladas
El agua hiperionizada tiene un estado hiperiónico, es decir, un equilibrio físicoquímico específico que implica la distribución de los iones disueltos, sus interacciones electrostáticas, su solvatación (interacción ión-molécula de agua) y parámetros electroquímicos (potencial redox/ORP, actividades iónicas, etc.).
Este estado puede alterarse cuando el agua circula por sistemas de filtración diseñados para el agua «convencional», porque algunos medios filtrantes hacen algo más que retener partículas: adsorben, intercambian o reconfiguran iones en la interfase sólido/agua. En este caso, el filtro se convierte en un actor químico capaz de neutralizar el estado hiperiónico.
Un filtro puede hacer algo más que «filtrar» : ciertos materiales interactúan con el agua y pueden eliminar gradualmente sus propiedades.
1) El principio clave : el estado hiperiónico es sensible a las interfaces sólidas
1.1 El agua no es "la misma" cerca de una superficie: la doble capa eléctrica
Cuando el agua entra en contacto con un sólido, se forma una doble capa eléctrica (EDL) :
- una capa de iones «ligados» a la superficie (capa de Stern),
- una capa difusa en la que los iones se distribuyen en función del potencial eléctrico.
Esta organización depende de la fuerza iónica del agua, definida por:
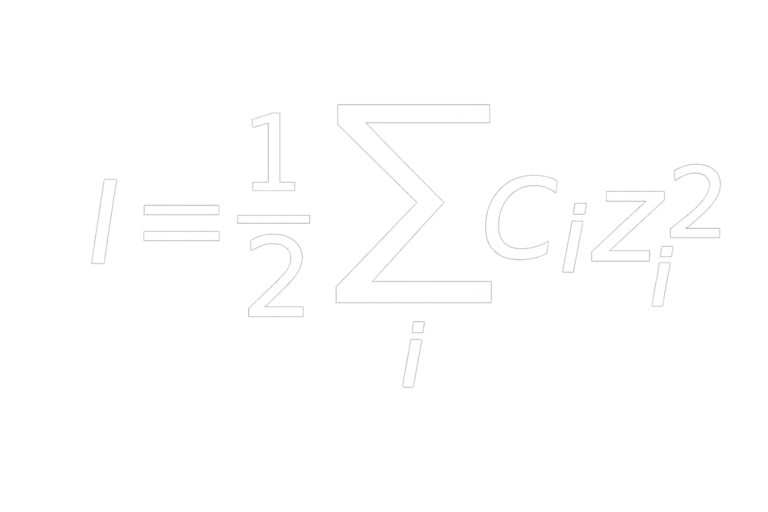
donde ci es la concentración molar del ion i y zi su valencia.
El «tamaño» típico de la zona interfacial electrostática es la longitud de Debye :
- εr : permitividad relativa del agua
- ε0 : permitividad del vacío
- kB : constante de Boltzmann
- T : temperatura (K)
- NA : Constante de Avogadro
- e : carga elemental
- I : fuerza iónica
Interpretación : cuanto más ionizada esté el agua ( I grande), más pequeño es λD: los efectos interfaciales están muy localizados pero son muy intensos.
Al entrar en contacto con un material, el agua se reorganiza formando una fina capa "eléctrica".
Cuanto más iones contenga el agua (por ejemplo, el agua de mar), mayores serán estos efectos.
1.2 Potencial electroquímico : por qué el equilibrio iónico puede ser "desplazado" por un medio
El comportamiento de un ion en el agua se rige por su potencial electroquímico:

- μi : potencial electroquímico
- μi0 : referencia
- R : constante de los gases perfectos
- ai : actividad del ion i
- F : Constante de Faraday
- ψ : potencial eléctrico local
La actividad es :
(γi : coeficiente de actividad, ci: concentración)
Punto crucial : cerca de una superficie, ψ ≠ 0 y cambia la distribución iónica. Si un medio filtra, adsorbe o intercambia iones, entonces ci, γi y, por ende, ai cambian. Esto desplaza el equilibrio que sustenta el estado hiperiónico.
Ciertos materiales "atraen" o "capturan" iones : esto cambia el equilibrio interno del agua, un poco como si se eliminaran ingredientes de una receta.
2) Por qué los medios a base de sílice (arena/vidrio/diatomita) son incompatibles
2.1 Sílice y vidrio: misma química superficial (grupos silanol)
La arena filtrante (cuarzo), las perlas de vidrio filtrante, la diatomita y muchos medios «minerales» afines comparten superficies ricas en grupos silanol:

Estos grupos se ionizan en función del pH :

Cuando la superficie lleva ≡SiO-, se vuelve negativa y atrae cationes:
- monovalentes : Na+, K+.
- divalentes : Ca2+, Mg2+
- acumulación iónica en la interfase,
- atrapamiento parcial o adsorción específica,
- cambios en las actividades locales,
- reorganización de la capa de agua interfacial (enlaces de hidrógeno y solvatación).
La arena y el vidrio no son neutros: sus superficies llevan cargas que atraen iones y alteran el agua que los atraviesa.
2.2 El efecto "superficie total" : por qué un filtro de arena neutraliza rápidamente el agua hiperiónica
Un lecho filtrante (arena o vidrio) combina:
- una gran superficie específica (agregados),
- tiempo de contacto elevado (lecho profundo),
- pasadas repetidas (recirculación piscina/spa).
Aunque la interacción «por cm²» sea débil, el efecto total se vuelve dominante, ya que la cantidad de puntos de interacción interfaciales es enorme.
La captura interfacial puede representarse mediante una cinética simplificada de tipo adsorción (esquema):
- q : cantidad adsorbida
- C : concentración en la solución
- θ : fracción de puntos ocupados
- ka, kd : constantes de adsorción/desorción
Si la superficie total es grande, la capacidad efectiva de «reorganización/captura» del filtro aumenta bruscamente.
Cuanta más superficie haya en contacto (arena fina, filtro grande, circulación continua), más "reacondiciona" el agua el medio... y más disminuyen sus propiedades.
2.3 Diatomita : un factor agravante
- más interfaces activas,
- efectos acelerados de captura/reorganización.
La diatomita es muy porosa, lo que amplifica aún más las interacciones con el agua, haciéndola especialmente desfavorable.
3) Zeolitas : intercambio iónico (medio "químico", no sólo filtrante)
3.1 Reacciones típicas de intercambio
Ejemplos esquemáticos:

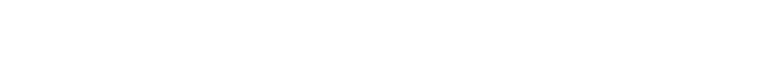
- la composición iónica (cationes),
- la fuerza iónica I,
- las actividades ai,
- los equilibrios asociados al estado hiperiónico.
Una zeolita actúa como una "esponja iónica" : transforma la química del agua intercambiando iones.
4) Carbón activado: adsorción masiva + impactos electroquímicos (ORP)
4.1 Adsorción : por qué altera el equilibrio
El carbón activado tiene una superficie específica muy elevada y adsorbe un gran número de especies disueltas.
Dos modelos clásicos :
Langmuir :
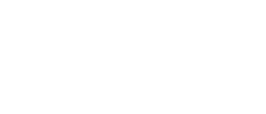
Freundlich :
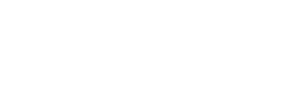
- q : masa adsorbida por masa de carbono
- C : concentración en la solución
- K, KF, n : constantes
La adsorción elimina las especies disueltas y desplaza los equilibrios de la solución.
Para un estado hiperiónico que depende de un equilibrio iónico/solución, es estructuralmente desfavorable.
El carbón activado está diseñado para "aspirar" lo que está disuelto. Sin embargo, para preservar un determinado estado del agua, es necesario evitar un material que elimine elementos constantemente.
4.2 ORP / redox : relación de Nernst
El potencial redox es el siguiente (para un par determinado):
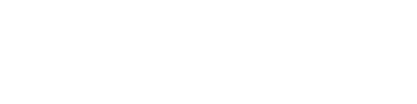
- E : potencial medido
- E0 : potencial estándar
- n : número de electrones intercambiados
- P : cociente de reacción
Las superficies de carbono pueden favorecer determinadas reacciones superficiales (adsorción + transferencia de electrones), modificando localmente Q y , por tanto, E.
Un medio también puede influir en el equilibrio "oxidante/reductor" del agua : esto puede contribuir a desestabilizar el estado deseado.
5) Regla de oro : "cuanto más eficaz es químicamente, más incompatible se vuelve".
Un medio filtrante de «alto rendimiento químico» (adsorción, intercambio iónico, superficie activa, microporosidad) no es neutro. El agua hiperionizada necesita un medio hidráulico y filtrante que filtre sin requimizar.
Los filtros que más modifican el agua (carbón, zeolita, sílice) son precisamente los que hay que evitar.
6) Medio compatible : filtración mecánica neutra
6.1 Polímeros PP/PE (polipropileno / polietileno)
- superficie relativamente neutra,
- sin intercambio estructural de iones,
- sin adsorción masiva,
- filtración por interceptación/cribado.
Los cartuchos de polímero retienen las partículas sin "capturar" los iones: conservan mejor el agua.
6.2 Celulosa (algodón/papel/fibras)
- eficaz con partículas,
- Las interacciones químicas suelen ser débiles en comparación con los medios minerales activos.
Los filtros de fibra actúan como un "tamiz fino" y respetan mejor el equilibrio del agua.
7) Recomendaciones prácticas (piscina, spa, talasoterapia, agua de mar)
- Piscinas / spas : se prefieren los cartuchos de PP/PE y/o los medios de fibra de celulosa.
- Agua de mar : mayor atención, ya que alta fuerza iónica → interacciones interfaciales más fuertes.
- Agua sanitaria / redes : busca estabilidad + neutralidad, evita los medios minerales activos.
Cuanto mayor sea el contenido en sal del agua (agua de mar), más filtración "neutra" se necesitará.
